コンテンツ
発表論文
最近の論文内容紹介
Ogawa, S., Kido, S., Handa, T., Ogawa, H., Asakawa, H., Takahashi, TS., Nakagawa, T., Hiraoka, Y., Masukata, H.
Regulation of mitotic recombination between DNA repeats in centromeres. The EMBO Journal, e98997, Published online 11.07.2018, doi: 10.15252/embj.201898997 (2018)
ホームページへ
細胞は、分裂して二倍になる前に、自身のもつ遺伝情報を複製します。細胞の遺伝情報を担う巨大な染色体DNAを限られた時間内に完全に複製するため、染色体上には多数の複製開始点が存在し、それらは領域毎に異なる時期(タイミング)に複製されます。これまで、複製タイミングは細胞核内の空間的配置と関係すると考えられてきましたが、そのしくみはまったく解っていませんでした。
本研究では、単細胞真核生物である分裂酵母を用いて、特定の複製開始点に目印となる蛍光タンパク質(LacI-GFP)を結合させる遺伝子操作を行うことにより、生きた細胞内で複製開始点の位置を解析することに成功しました。その結果、後期に複製を開始する複製開始点だけが核膜に局在することを発見し、さらにそれらは複製タイミングが決定されるG1/S時期にはテロメアに隣接する位置に移動することを発見しました。種々の遺伝子欠損株を用いた解析から、核膜に局在することは複製タイミング制御には重要ではなく、G1/S期にテロメアに隣接することが重要であると結論しました。またテロメアに結合して末端保護とテロメア長制御にはたらくシェルタリン(shelterin)と呼ばれるタンパク質複合体が、複製開始点をテロメアに引き寄せて複製タイミングを制御するしくみにはたらくことを発見しました。本研究は、染色体末端テロメアが遠く離れた染色体内部とコミュニケーションするしくみを明らかにしたことになり、将来テロメアが遠隔制御する疾患原因遺伝子の発見につながる可能性があります。
Terui, R., Nagao, K., Kawasoe, Y., Taki, K., Higashi, TL., Tanaka, S., Nakagawa, T., Masukata, H., Takahashi, TS.
Nucleosomes around a mismatched base pair are excluded via an Msh2-dependent reaction with the aid of SNF2 family ATPase Smarcad1. Genes and Development, vol. 32: 806-821, Published in Advance June 13, 2018, doi: 10.1101/gad.310995.117 (2018)
ホームページへ
Zafar, F., Okita, AK., Onaka, AT., Su, J., Katahira, Y., Nakayama, J., Takahashi, TS., Masukata, H., Nakagawa, T.
Regulation of mitotic recombination between DNA repeats in centromeres. Nucleic Acids Research, vol. 45(19), 11222-11235, doi.org/10.1093/nar/gkx763 (2017)
ホームページへ
Onaka, AT., Toyofuku, N., Inoue, T., Okita, AK., Sagawa, M., Su, J., Shitanda, T., Matsuyama, R., Zafar, F., Takahashi, TS., Masukata, H., Nakagawa, T.
Rad51 and Rad54 promote noncrossover recombination between centromere repeats on the same chromatid to prevent isochromosome formation. Nucleic Acids Research, doi:10.1093/nar/gkw874 (2016)
ホームページへ
不思議なことに真核生物のゲノムには数多くのリピート配列が存在します。こうしたリピート配列を「のりしろ」にして染色体異常が起こります。しかし、異常染色体が生じると細胞死や遺伝病など深刻な問題が生じます。相同組換え因子であるヒトBRCA2に変異があると、高頻度に染色体異常を起こし乳がんになるリスクが高くなります。これまでに我々も、相同鎖交換反応を触媒するRad51に変異があるとセントロメア・リピートを介した染色体異常が高頻度に起こることを見つけました。こういったことから、相同組換えは染色体の安定維持に重要であると考えられます。しかし、相同組換えがどの様にしてリピート配列、つまり、相同配列を介した染色体異常を防ぐのかは謎でした。ただ、相同組換えには局所的な変化しか起きない「非交叉型組換え」とDNA鎖の乗り換えを起こす「交叉型組換え」があります。本論文では、Rad51がモーター蛋白質Rad54と共にセントロメア・リピート間での「非交叉型組換え」を促進することを明らかにしました。また、そうすることでDNA切断酵素Mus81によって起こる「交叉型組換え」を介した染色体異常を抑制することが分かりました。今回の研究により、Rad51, Rad54による染色体異常の抑制メカニズムが明らかになりました。また、今後Mus81の阻害剤を発見することで乳がんの治療薬を開発する道筋を開いたと考えられます。
Kawasoe, Y., Tsurimoto, T., Nakagawa, T., Masukata, H., Takahashi, TS.
MutSα maintains the mismatch repair capability by inhibiting PCNA unloading. eLIFE, 12;5:e15155. doi: 10.7554/eLife.15155 (2016)
ホームページへ
細胞が増えるためには、DNAにコードされた遺伝情報をコピーする必要がありますが、このときコピーの誤りが生じることがあります。これを直さずにおくと、遺伝情報の変化(変異)が起こります。ミスマッチ修復は、このコピーの誤りを修復するための重要なDNA修復機構です。ミスマッチを直すためには、正しい情報を持つ古いDNA鎖と、誤って合成された新しいDNA鎖を区別する必要があります。鎖の新旧を区別するためには、コピーを取る過程の情報を得ることが必要です。DNA複製の際には、まずPCNAと呼ばれるリング型分子がDNAに装着されます。次にPCNAを足場にDNA合成酵素が結合し、新しいDNA鎖が合成されます。PCNAは役割を終えると速やかにDNAから外されます。PCNAにはDNA合成酵素が結合する面があり、この面を見分けることで、古い鎖と新しい鎖の情報を得ることができると予想されます。PCNAが新旧鎖の情報をミスマッチ修復に伝える分子であるという仮説はこれまで提唱されていましたが、その証明はありませんでした。またPCNAはDNA合成が終わるとすぐDNAから外されてしまうため、PCNAが新旧鎖の情報を持つとしても、どのようにしてそれをミスマッチ修復に伝えることができるのかは謎でした。本研究では、ツメガエル卵抽出液をモデル系に使って試験管内でミスマッチ修復を再現し、DNA複製に必要なタンパク質である、複製クランプ(PCNA)が新旧鎖を区別する情報を持つことを実験的に証明しました。さらに、ミスマッチ修復はPCNAがDNAから外されてしまうのを防止して鎖の情報を長時間保持することを発見しました。
Tashiro, T., Handa, T., Matsuda, A., Ban, T., Takigawa, T., Miyasato, K., Ishii, K., Kugou, K., Ohta, K., Hiraoka, Y., Masukata, H., Kanoh, J.
Shugoshin forms a specialized chromatin domain at subtelomeres that regulates transcription and replication timing. Nature Communications, 12;5:e15155. doi: 10.7554/eLife.15155 (2016).
ホームページへ
真核生物で広く保存されているシュゴシンタンパク質(Sgo2)は、M期セントロメアに局在して染色体を均等に分配する制御に関わることが知られている。我々は、阪大蛋白質研究所の加納純子准教授、生命機能研究科の平岡泰教授、東大総合文化研究科の太田邦史教授らのグループと共に、Sgo2の間期染色体における新たな役割を解明した。分裂酵母染色体では末端のテロメアに接するサブテロメア領域(約50-100kbに及ぶ)は多くの遺伝子が発現抑制されており、またDNAの複製は後期に複製するように制御されている。Sgo2はM期にはセントロメアに局在するが、間期になるとサブテロメアに局在してKnob(ブ)と呼ばれる高次に凝縮されたクロマチン構造形成に関与する。サブテロメアでSgo2はヘテロクロマチン構造とは独立に遺伝子の転写を抑制することを発見した。さらにサブテロメアの複製開始点の複製タイミングを後期にするしくみに関与することを見いだした。従来M期での重要な働きが知られていたSgo2であるが、間期でもサブテロメアで多様な機能を果たすという発見により、Sgo2が染色体機能の維持に多面的に関与することが示された。このようなしくみは分裂酵母以外の生物種でも存在するのではないか。
Tazumi, A., Fukuura, M., Nakato, R., Kishimoto, A., Takenaka, T., Ogawa, S., Song, J., Takahashi, TS., Nakagawa, T., Shirahige, K., Masukata, H.
Telomere-binding protein Taz1 controls global replication timing through its localization near late replication origins in fission yeast. Genes Dev., 26 (18), 2050-2062 (2012) doi: 10.1101/gad.194282.112
ホームページへ
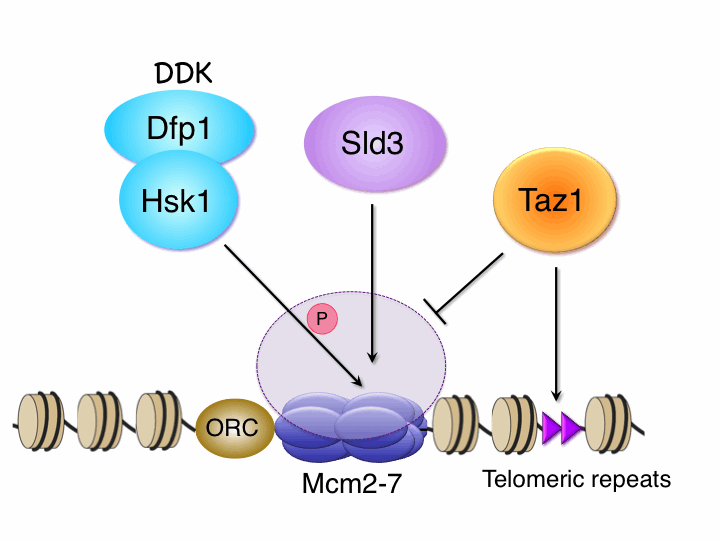
真核生物では長大な染色体DNAを限られた時間内に複製するために、多数の複製開始点が存在する。興味深いことにそれぞれの複製開始点はS期の特定の時期に複製を開始するようプログラムされている。我々は染色体上の全複製開始点が同定されている分裂酵母を用いて、複製タイミングプログラムの決定機構を解析した。染色体腕部のLate origin(S期初期に複製しない開始点)の複製タイミング制御には、その近傍に存在する2コピーのテロメアリピート配列が必須であることを見いだした。染色体末端でテロメアリピートに直接結合し他のタンパク質と相互作用してテロメア長制御に機能するTaz1(ヒトTRF1, TRF2ホモログ)が、染色体内部のLate origin近傍のテロメア配列にも結合し、複製タイミング制御に必須の役割を果たすことを発見した。全ゲノムレベルの解析により、約半数のLate originがTaz1依存的制御下にあることが明らかとなり、テロメア結合タンパク質が複製タイミングプログラムに重要な役割を果たすことが示された。
Handa, T., Kanke, M., Takahashi, TS., Nakagawa, T., Masukata, H.
DNA polymerization-independent functions of DNA polymerase epsilon in assembly and progression of the replisome in fission yeast. Mol. Biol. Cell, 23 (16), 3240-3253 (2012) doi: 10.1091/mbc.E12-05-0339
ホームページへ
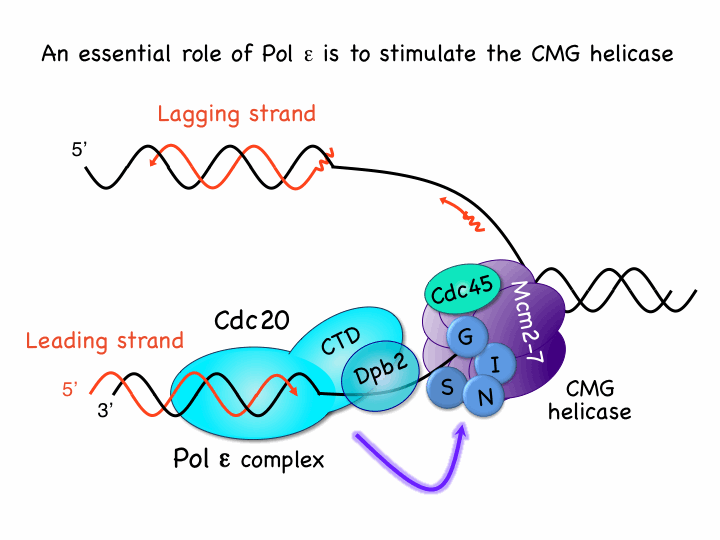
真核生物染色体DNAを複製する複製フォークでは、DNA二重鎖がCMG (Cdc45-MCM-GINS) ヘリカーゼ複合体によってほどかれ、各一本鎖DNAを鋳型として、片方の鎖は連続的に合成され(Leading鎖)、他方はOkazaki fragments として不連続に合成される(Lagging鎖)。Leading鎖DNAはDNA Pol epsilon複合体が合成し、Lagging鎖はPol alpha-primase複合体が合成したRNA-DNAプライマーを、Pol delta複合体が伸長する。これら3つのポリメラーゼは、すべて生存に必須で保存されている。ところが興味深いことに、Pol epsilonの触媒サブユニットCdc20/Pol2には他のポリメラーゼには無い巨大なC末端ドメイン(CTD)が存在し、N末ポリメラーゼドメインは欠失できるのに対しCTDは生存に必須である。出芽酵母では、Pol epsilonは複製開始前にCMG複合体形成に必要であると示されているが、それではPol epsilonは複製フォークでは必須ではないのだろうか? 我々は、複製フォークにおけるPol epsilonの必須機能を明らかにするために分裂酵母をモデル生物として解析した。分裂酵母Cdc20のCTDに変異を導入して得た高温感受性変異株では、制限温度においてもCMGヘリカーゼが活性化され、Pol alpha、Pol deltaが結合して複製を開始したが、CMGヘリカーゼは複製開始点から移動できないことが明らかとなった。これらの結果から、Cdc20-CTDはCMGヘリカーゼを促進する機能を持つことが示唆された。リーディング鎖ポリメラーゼPol epsilonによるリーディング鎖DNA合成は他のポリメラーゼによって代替可能であるが、CMGヘリカーゼ活性促進は必須である。リーディング鎖ポリメラーゼが停止時にヘリカーゼを減速させることは、過度の一本鎖DNA形成を抑制し、染色体の異常を抑える役割を持つと考えられる。
Higashi, T. L., Ikeda, M., Tanaka, H., Nakagawa, T., Bando, M., Shirahige, K., Kubota, Y., Takisawa, H., Masukata, H., Takahashi, T. S.
The Prereplication Complex Recruits XEco2 to Chromatin to Promote Cohesin Acetylation in Xenopus Egg Extracts. Curr. Biol., 22, 977-988 (2012), (doi: 10.1016/j.cub.2012.04.013)
ホームページへ
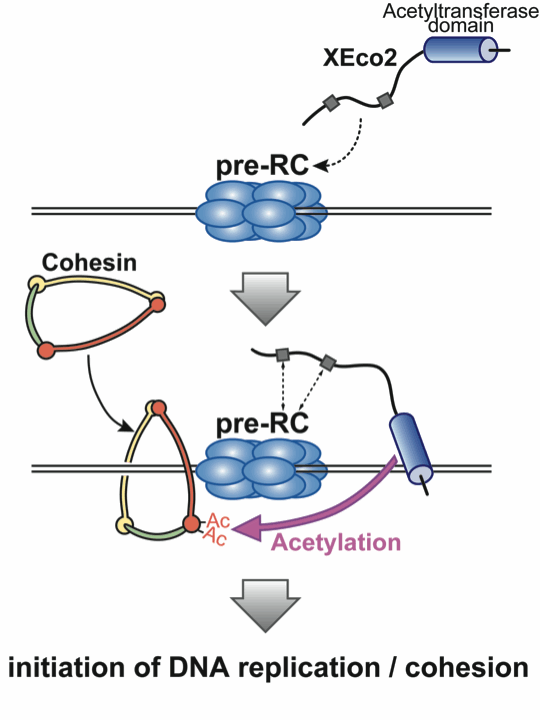
真核細胞は細胞周期のS期に染色体を複製し、M期に染色体分配を行います。S期に合成される姉妹染色体は、DNA複製に伴ってコヒーシン複合体により接着されます。この染色体接着により、M期での正確な染色体分配が可能になります。従って染色体接着は染色体の複製と分配を結びつける反応と言えます。コヒーシンはDNA複製開始の前にDNAに結合し、DNA複製の進行に伴って接着に必須のアセチル化修飾を受けると考えられてきました。アセチル化修飾の機能はまだ正確に分かっていませんが、アセチル化によりコヒーシン分子のDNA結合が安定化されることが示唆されています。このアセチル化はコヒーシンアセチル基転移酵素(CoAT)と呼ばれる酵素が担っており、脊椎動物は二種類のCoATを持ちます。本論文では、アフリカツメガエル卵抽出液を脊椎動物のモデル系に用いて、DNA複製開始に必要な複製開始前複合体(pre-RC)がCoATによるコヒーシンのアセチル化に必要であることを発見しました。ツメガエルCoATであるXEco1とXEco2の解析から、初期胚ではXEco2のみがコヒーシンアセチル化に必要である事、およびXEco1は初期胚で発現しておらず体細胞で優先的に発現していることが分かりました。興味深いことに、XEco2の染色体結合とコヒーシンのアセチル化はpre-RC形成に依存しており、DNA合成の開始前から効率よく起こっていました。pre-RC形成に依存したXEco2の染色体結合を失わせると、コヒーシンのアセチル化と染色体接着が完全に失われました。さらに、コヒーシンのDNA結合の安定化には、アセチル化だけでなくDNA複製反応が必要でした。これらの研究成果から、ツメガエル初期胚ではpre-RCの形成がコヒーシンのアセチル化とDNA複製の開始を協調させること、および、コヒーシンのアセチル化に加えてDNA複製時に起こる未知の反応がコヒーシンのDNA結合安定化に必要であることが分かりました。我々は以前にpre-RCに結合するDDK複合体がコヒーシン複合体のローディングに機能する事を発見しており(Takahashi et al., Genes Dev. 2008)、pre-RCは染色体複製開始の場であるとともに、コヒーシンとXEco2の染色体結合、コヒーシンアセチル化の場でもあり、染色体接着に必要な因子を複製開始の場に供給する役割を果たしていると考えています。
Kanke, M., Kodama, Y., Takahashi, TS., Nakagawa, T., Masukata, H.
Mcm10 plays an essential role in origin DNA unwinding after loading of the CMG components. The EMBO Journal, 31, 2182-2194 (2012) doi:10.1038/emboj.2012.68, Published online 20 March 2012.
ホームページへ
DNAを複製するためには、DNAをほどくDNAヘリカーゼの活性が重要である。真核生物のDNAヘリカーゼであるMCM複合体は、G1期に開始点に結合してpre-RCを形成し、S期になりGINS、Cdc45などの因子が結合してヘリカーゼとして活性化する。複製フォークではGINS、Cdc45、MCM複合体から構成されるCMG (Cdc45-MCM-GINS)複合体が複製ヘリカーゼとして働くと考えられている。MCM複合体はpre-RCでは二重鎖DNAにdouble hexamerとして結合しているが、複製フォークでは一本鎖DNAにsingle hexamerとして結合していると考えられている。しかし、どのようにしてその変化が起こるのかはよく分かっていない。Mcm10はMCM複合体と強い物理的・遺伝学的相互作用を持つことから、Mcm10の機能を解明することによりMCMヘリカーゼ活性化メカニズムを理解できるのではないかと考えた。我々は転写抑制と条件誘導蛋白質分解系を用いてMcm10を分裂酵母細胞から除去し、複製開始反応がどこまで進むか解析した。その結果、Mcm10がなくても複製開始点上にCMG構成因子が結合したが、開裂した一本鎖DNAに結合するRPAやDNAポリメラーゼα、艪フ結合が大幅に減少した。興味深いことに、Mcm10の保存されたzinc fingerモチーフに変異を導入した変異Mcm10は、複製開始点に結合するがRPAの結合を誘起しなかった。またこの変異はMcm10同士の相互作用と一本鎖DNA結合活性を低下させた。我々は、Mcm10が多量体としてCMG複合体に結合してMCMの構造をdouble hexamerからsingle hexamerへと変化させ、さらに一本鎖DNA結合活性によってDNA 二重鎖開裂を安定化することにより、DNA複製開始に必須の役割を果たすのではないかと考えている。

Maki, K., Inoue, T., Onaka, A., Hashizume, H., Somete, N., Kobayashi, Y., Murakami, S., Shigaki, C., Takahashi, TS., Masukata, H., Nakagawa, T.
Abundance of prereplicative complexes (Pre-RCs) facilitates recombinational repair under replication stress in fission yeast. J. Biol. Chem., 286(48), 41701-41710 (2011)
ホームページへ
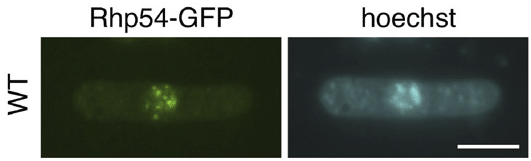
DNA複製ヘリカーゼであるMcm2-7は複製の開始前に染色体に結合してpre-RC複合体を形成する。酵母からヒトに至るまで真核生物では染色体あたり数多くの部位でpre-RCが形成され、ゲノム全体では数百〜数千にも達すると考えられている。実はpre-RCを多数形成することはS期の間に速やかに染色体を倍加するだけでなくゲノム維持や分化・発生にも関与することが知られている。このようにpre-RCはDNA複製に限らず様々な生命現象に影響するが、そのメカニズムについては解明されていない。我々はpre-RCが減少する分裂酵母mcm6-S1変異株を単離し、DNAダメージ応答について詳細に解析した。その結果、mcm6-S1変異株ではチェックポイントの活性化や組換え修復の開始は正常に起こるが、組換え後期過程に働く Rhp54/Rad54が核に蓄積することが分かった。重要なことに、このRhp54の蓄積は人為的にpre-RC の数を増加させることで解消された。我々はこれらの結果をもとに、pre-RCの多数形成が多数の複製開始を保障することでSynthesis- dependent strand annealing (SDSA)タイプの組換え反応を促進するモデルを提唱した。
Fukuura, M., Nagao, K. Obuse, C., Takahashi, TS., Nakagawa, T., Masukata, M.
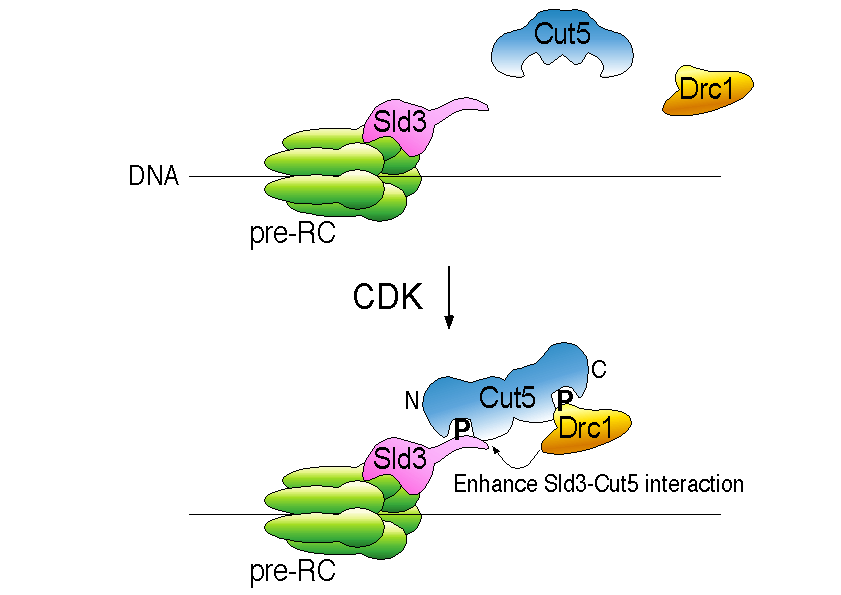
CDK promotes interactions of Sld3 and Drc1 with Cut5 for initiation of DNA replication in fission yeast. Molecular Biology of the Cell, 22(14), 2620-2633 (2011)
ホームページへ
真核生物の染色体DNAは細胞周期のS期にすべての領域がただ1回のみ複製する。この複製開始制御に必須の役割を果たすのがCyclin-dependent kinase (CDK)である。我々は分裂酵母を用いて複製開始因子Sld3とSld2/Drc1がCDKによってリン酸化されることを示し、それぞれのリン酸化に依存的にCut5/Dpb11/TopBP1の2箇所のBRCTドメインと結合し、三者複合体を形成することが、複製開始に必須であることを明らかにした。このようなCDK依存的制御機構は出芽酵母-分裂酵母でよく保存されていることが示唆された。
Kanke, M., Nishimura, K., Kanemaki, M., Kakimoto, T., Takahashi, TS., Nakagawa, T., Masukata, H.
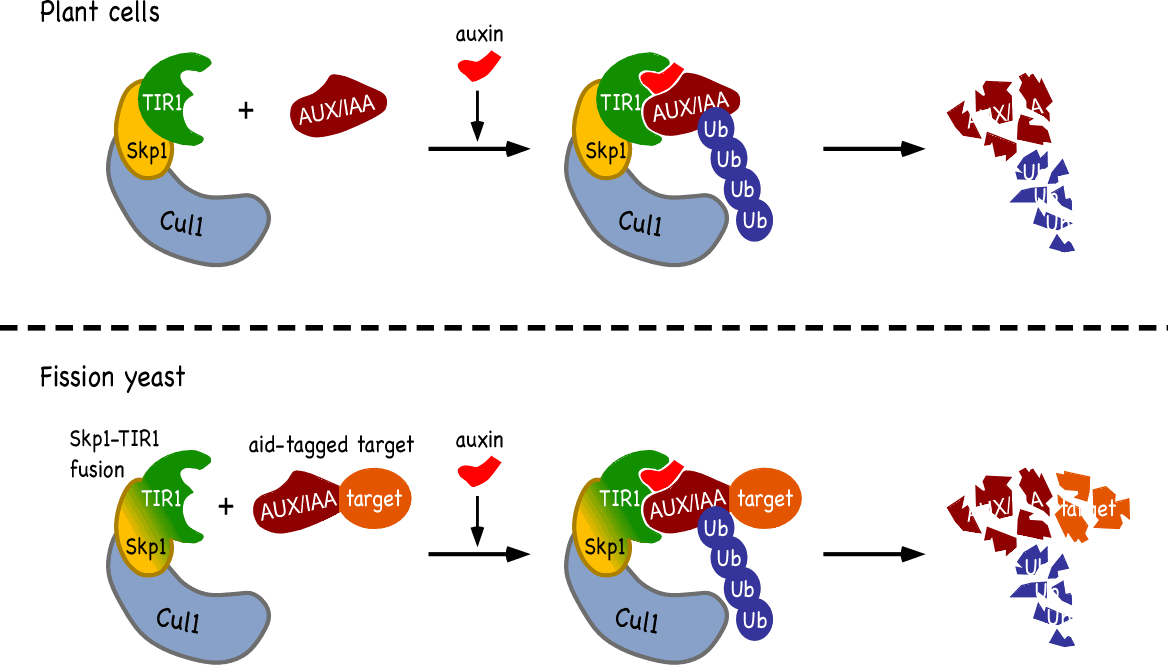
Auxin-inducible protein depletion system in fission yeast. BMC Cell Biology, 12:8, doi:10.1186/1471-2121-12-8 (2011)
ホームページへ
細胞内で必須遺伝子の機能を解析する手法として、タンパク質を条件誘導的に分解する"デグロン"法は必須遺伝子の機能解析に有効であるが、これまでモデル生物分裂酵母では効率よくタンパク質を分解するシステムがなかった。われわれは、植物ホルモン「オーキシン」を添加すると標的タンパク質を特異的にユビキチン化し分解する'Auxin-inducible degron"を分裂酵母で構築し、標的遺伝子の転写抑制と組み合わせることによって、迅速かつ効率的にタンパク質をほぼ完全に除去する"off-AID" systemを開発することに成功した。
Hayashi, T.M., Takahashi, S.T., Nakagawa, T., Nakayama, J., Masukata, H.
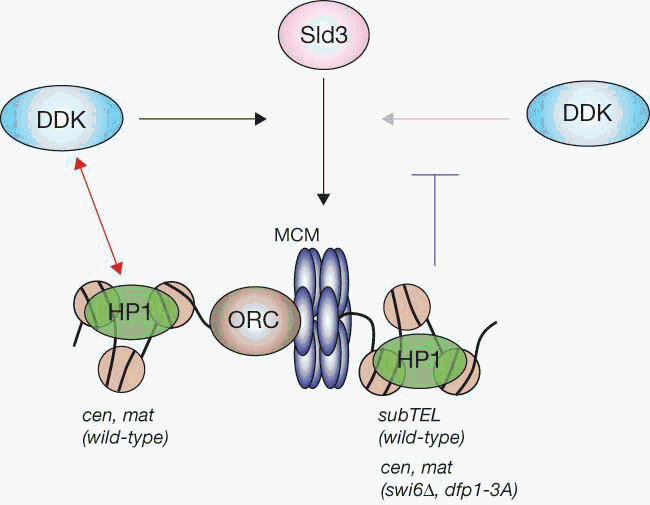
The heterochromatin protein Swi6/HP1 activates replication origins at the pericentromeric region and silent mating-type locus. Nature Cell Biology, 11, 537-562 (2009), (DOI:10.1038/ncb1845)
ホームページへ
真核生物染色体の各領域はそれぞれS期の決まった時期に複製する。凝縮した構造で遺伝子発現が抑制されているヘテロクロマチン領域は一般に遅い時期に複製する。しかしながら分裂酵母のセントロメア外縁と性決定領域では、ヘテロクロマチンタンパク質Swi6(ヒトのHP1)が複製開始点を活性化しS期の初期に複製させることを解明した。初期複製するヘテロクロマチンではSwi6はDfp1(複製開始に必要なタンパク質リン酸化酵素の構成因子)をヘテロクロマチンにリクルートすることにより、Sld3という複製開始因子がヘテロクロマチン領域の複製開始点に結合することを促進するという分子メカニズムを解明した。
Nakamura, KI., Okamoto, A., Katou, Y., Yadani, C., Shitanda, T., Kaweeteerawat, C., Takahashi, TS., Itoh, T., Shirahige, K., Masukata, H., Nakagawa, T.
Rad51 suppresses gross chromosomal rearrangement at centromere in Schizosaccharomyces pombe. EMBO Journal, 27, 3036-3046 (2008)
ホームページへ
遺伝情報を正確に娘細胞に伝えるためには染色体を安定に維持することが必要である。その為には外的あるいは内的要因により染色体DNAが傷害を受けた場合にも、それを適切に処理して転座、逆位などの染色体異常を防がなければならない。DNA相同組換えは二重鎖切断などの重篤なDNA傷害を直すことができる修復システムである。ヒト乳癌の研究などから、相同組換えが染色体の安定維持に重要な役割を果たすことが示されている。ただし、その分子メカニズムは明らかでない。そこで、我々は相同組換えがどのようにして染色体異常を抑制するのかを知るために分裂酵母S. pombeを用いて染色体異常を検出する新たな実験系を構築した。そして、相同組換えに於いて中心的役割を果たすRad51を破壊した酵母株を作成してその影響を調べた。その結果、rad51破壊株では染色体異常が野生株に比べて高頻度に起こることが分かった。また、rad51破壊株で生じた異常染色体の構造を詳細に調べたところ、染色体セントロメア領域で再編を起こした同腕染色体(Isochromosome)と呼ばれる異常染色体が主に観察された。このことから、Rad51がセントロメアで機能する可能性が考えられる。そこで、Rad51蛋白の染色体結合についてクロマチン免疫沈降法により解析した。その結果、Rad51が細胞周期のS期周辺でセントロメアに結合することが分かった。これらの結果から、特殊な染色体クロマチン高次構造をとるセントロメアの安定維持に相同組換えが重要な役割を果たすと考えられる。
Nitani, N., Yadani, C., Yabuuchi, H., Masukata, H. and Nakagawa, T.
Mcm4 C-terminal domain of MCM helicase prevents excessive formation of single-stranded DNA at stalled replication forks. Proc. Natle. Acad. Sci.USA 105 (35), 12973-12978 (2008)
ホームページへ
遺伝情報を娘細胞に正確に受け継ぐためには染色体DNAを完全に複製することが必要である。ところが、細胞内ではDNA複製の進行は様々な要因により阻害されることが知られている。このとき、複製フォークは構造変化を起こすことで複製チェックポイントの活性化を誘導し、それにより複製フォークの崩壊や細胞周期の無秩序な進行などが抑制されている。しかし、複製フォークの構造変化がどのようにコントロールされているか、その分子機構は明らかでなかった。そこで、我々は複製進行に働くMCMヘリケースに着目し、その役割を分裂酵母S. pombeを用いて解析した。その結果、Mcm4サブユニットのC末領域(Mcm4 CTD)が複製停止時に過剰に単鎖DNAが形成することを防ぐ、謂わば、MCMヘリケースの分子ブレーキの役割を果たすことを明らかにした。Mcm4 CTDのアミノ酸配列は古細菌からヒトまで保存されていることから、そのブレーキとしての役割も広く真核生物に保存されていると予想される。また、近年、マウスを使った実験からMcm4の変異により染色体異常が増大し、乳癌が誘発されることが報告された。したがって、今回の研究により得られたMCMヘリケースに関する知見は癌などの遺伝病の原因解明にも貢献すると考えられる。
Takahashi, T.S., Basu, A., Bermudez. V., Hurwitz. J. and Walter, J.C.
Cdc7-Drf1 kinase links chromosome cohesion to the initiation of DNA replication in Xenopus egg extracts. Genes Dev. 22 (14), 1894-1905 (2008)
ホームページへ
Cdc7タンパク質リン酸化酵素が染色体の複製と分配を結びつけていることを発見: 正確な染色体の複製と分配は、共に細胞の増殖に必須である。真核生物では、染色体を正確に分配するために、複製された二つの姉妹染色体をコヒーシン分子によって接着している。姉妹染色体の接着はDNA複製と同時に起こる。一方、コヒーシン分子の染色体結合がどのように制御されているかはよく分かっていなかった。本論文では、アフリカツメガエル(Xenopus laevis)の卵抽出液をモデル系に用いて、Cdc7タンパク質リン酸化酵素がコヒーシンの染色体結合に重要な機能を持つことを発見した。Cdc7はDNA複製開始に必須の因子であることが既に分かっている。従ってこの発見は、高等動物ではDNA複製の開始と姉妹染色体の接着という二つの反応が、Cdc7の機能により密接に連携していることを示している。
Hayashi, M., Katou, Y., Itoh, T., Tazumi, A., Yamada, Y., Takahashi, T., Nakagawa, T., Shirahige, K. and Masukata, H.
Genome-wide localization of pre-RC sites and identification of replication origins in fission yeast. EMBO J. 26, 1327-1339 (2007); doi: 10.1038/sj.emboj.7601585
ホームページへ染色体は特定の場所から特定の時期に複製することによって染色体全体が完全に複製されるように制御されている。このしくみを明らかにするために分裂酵母Schizosaccharomyces pombeの複製開始点を網羅的に決定した。複製因子Orc1とMcm6の結合部位をクロマチン免疫沈降法(ChIP)と高密度DNAタイリングアレイにより460個の複製開始点を決定し、さらにS期初期の複製領域をブロモデオキシウリジン(BrdU)で標識しアレイ解析した結果、307個が初期に複製することを示した。また後期複製開始点がチェックポイントで制御されることを示した。セントロメアやテロメアのヘテロクロマチン領域の複製は独自の制御を受けていることが明らかとなった。
論文リスト
Zafar, F., Okita, AK., Onaka, AT., Su, J., Katahira, Y., Nakayama, J., Takahashi, TS., Masukata, H., Nakagawa, T.
Regulation of mitotic recombination between DNA repeats in centromeres. Nucleic Acids Research, vol. 45(19), 11222-11235, doi.org/10.1093/nar/gkx763 (2017)
ホームページへ
Onaka, AT., Toyofuku, N., Inoue, T., Okita, AK., Sagawa, M., Su, J., Shitanda, T., Matsuyama, R., Zafar, F., Takahashi, TS., Masukata, H., Nakagawa, T.
Rad51 and Rad54 promote noncrossover recombination between centromere repeats on the same chromatid to prevent isochromosome formation. Nucl Acids Res., doi:10.1093/nar/gkw874 (2016).
ホームページへ
Kawasoe, Y., Tsurimoto, T., Nakagawa, T., Masukata, H., Takahashi, TS.
MutSα maintains the mismatch repair capability by inhibiting PCNA unloading. eLIFE, 12;5:e15155. doi: 10.7554/eLife.15155 (2016).
ホームページへ
Johnson, C., Gali, VK., Takahashi, TS., Kubota, T.
PCNA retention on DNA into G2/M phase causes genome instability in cells lacking Elg1. Cell Rep., 19;16(3):684-695. doi: 10.1016/j.celrep.2016.06.030. (2016).
ホームページへ
Tashiro, T., Handa, T., Matsuda, A., Ban, T., Takigawa, T., Miyasato, K., Ishii, K., Kugou, K., Ohta, K., Hiraoka, Y., Masukata, H., Kanoh, J.
Shugoshin forms a specialized chromatin domain at subtelomeres that regulates transcription and replication timing. Nature Communications, 7:10393. doi: 10.1038/ncomms10393 (2016).
ホームページへ
Ruan, K., Yamamoto, TG., Asakawa, H., Chikashige, Y., Kimura, H., Masukata, H., Haraguchi, T., Hiraoka, Y.
Histone H4 acetylation required for chromatin decompaction during DNA replication. Scieitific Reports, 30;5:12720. doi: 10.1038/srep12720, (2015).
ホームページへ
Shintomi, K., Takahashi, TS., Hirano, T..
Reconstitution of mitotic chromatids with a minimum set of purified factors. Nat Cell Biol, 17(8):1014-1023. doi: 10.1038/ncb3187. (2015).
ホームページへ
Sanuki, Y., Kubota, Y., Kanemaki, MT., Takahashi, TS., Mimura, S., Takisawa, H.
RecQ4 promotes the conversion of the pre-initiation complex at a site-specific origin for DNA unwinding in Xenopus egg extracts. Cell Cycle, 114, 1010-1023. doi: 10.1080/15384101.2015.1007003 (2015).
ホームページへ
Ruan, K., Yamamoto, TG., Asakawa, H., Chikashige, Y., Masukata, H., Haraguchi, T., Hiraoka, Y.
Meiotic nuclear movements in fission yeast are regulated by the transcription factor Mei4 downstream of a Cds1-dependent replication checkpoint pathway. Genes to Cells., 20(3), 160-172. doi: 10.1111/gtc.12207, (2015).
ホームページへ
Slenn, TJ., Morris, B., Havens, CG., Freeman, RM., Takahashi, TS., Walter, JC.
Thymine DNA glycosylase is a CRL4Cdt2 substrate. J Biol Chem., 289(33): 23043–23055 (2014), doi: 10.1074/jbc.M114.574194
ホームページへ
Nanbu, T., Takahashi, K., Murray, JM., Hirata, N., Ukimori, S., Kanke, M., Masukata, H., Yukawa, M., Tsuchiya, E., Ueno, M.
Fission yeast RecQ helicase Rqh1 is required for the maintenance of circular chromosomes. Mol Cell Biol., 33 (6), 1175-1187 (2013), doi: 10.1128/MCB.01713-12
ホームページへ
Tazumi, A., Masukata, H.
Telomere-binding proteins play roles in control of replication timing. Cell Cycle, 11 (24), 4492-4493 (2012) doi: 10.4161/cc.22727
ホームページへ
Tazumi, A., Fukuura, M., Nakato, R., Kishimoto, A., Takenaka, T., Ogawa, S., Song, J., Takahashi, TS., Nakagawa, T., Masukata, H.
Telomere-binding protein Taz1 controls global replication timing through its localization near late replication origins in fission yeast. Genes Dev., 26 (18),2050-2062 (2012) doi: 10.1101/gad.194282.112
ホームページへ
Handa, T., Kanke, M., Takahashi, TS., Nakagawa, T., Masukata, H.
DNA polymerization-independent functions of DNA polymerase epsilon in assembly and progression of the replisome in fission yeast. Mol. Biol. Cell, 23 (16), 3240-3253 (2012) doi: 10.1091/mbc.E12-05-0339
ホームページへ
Higashi, T. L., Ikeda, M., Tanaka, H., Nakagawa, T., Bando, M., Shirahige, K., Kubota, Y., Takisawa, H., Masukata, H., Takahashi, TS.
The Prereplication Complex Recruits XEco2 to Chromatin to Promote Cohesin Acetylation in Xenopus Egg Extracts. Curr. Biol., 22, 977-988 (2012), doi: 10.1016/j.cub.2012.04.013
ホームページへ
Kanke, M., Kodama, Y., Takahashi, TS., Nakagawa, T., Masukata, H.
Mcm10 plays an essential role in origin DNA unwinding after loading of the CMG components. The EMBO Journal, 31, 2182-2194 (2012) Published online 20 March 2012, doi:10.1038/emboj.2012.68
ホームページへ
Maki, K., Inoue, T., Onaka, A., Hashizume, H., Somete, N., Kobayashi, Y., Murakami, S., Shigaki, C., Takahashi, TS., Masukata, H., Nakagawa, T.
Abundance of prereplicative complexes (Pre-RCs) facilitates recombinational repair under replication stress in fission yeast. J. Biol. Chem., 286(48), 41701-41710 (2011)
ホームページへ
Fukuura. M., Nagao. K. Obuse, C., Takahashi, TS., Nakagawa, T., Masukata, M.
CDK promotes interactions of Sld3 and Drc1 with Cut5 for initiation of DNA replication in fission yeast. Molecular Biology of the Cell, 22(14), 2620-2633 (2011)
ホームページへ
Kanke, M., Nishimura, K., Kanemaki, M., Kakimoto, T., Takahashi, TS., Nakagawa, T., Masukata, H.
Auxin-inducible protein depletion system in fission yeast. BMC Cell Biology, 12:8, doi:10.1186/1471-2121-12-8 (2011)
ホームページへ
Hayashi, MT. and Masukata, H.
Regulation of DNA replication by chromatin structures: accessibility and recruitment. Chromosoma, 120,(1), 39-46, DOI: 10.1007/s00412-010-0287-4 (2011)
ホームページへ
Sherwood, R., Takahashi, T.S., and Jallepalli, P.V.
Sister acts: coordinating DNA replication and cohesion establishment. Genes Dev., 24, 2723-2731 (2010)
ホームページへ
Hayashi, T.M., Takahashi, S.T., Nakagawa, T., Nakayama, J., Masukata, H.
The heterochromatin protein Swi6/HP1 activates replication origins at the pericentromeric region and silent mating-type locus. Nature Cell Biology, 11, 357 - 362,doi:10.1038 (2009)
ホームページへ
Nakamura, KI., Okamoto, A., Katou, Y., Yadani, C., Shitanda, T., Kaweeteerawat, C., Takahashi, TS., Itoh, T., Shirahige, K., Masukata, H., Nakagawa, T.
Rad51 suppresses gross chromosomal rearrangement at centromere in Schizosaccharomyces pombe. EMBO Journal, 27, 3036-3046 (2008)
ホームページへ
Nitani, N., Yadani, C., Yabuuchi, H., Masukata, H. and Nakagawa, T.
Mcm4 C-terminal domain of MCM helicase prevents excessive formation of single-stranded DNA at stalled replication forks. Proc. Natle. Acad. Sci.USA 105 (35), 12973-12978 (2008)
ホームページへ
Takahashi, T.S., Basu, A., Bermudez. V., Hurwitz. J. and Walter, J.C.
Cdc7-Drf1 kinase links chromosome cohesion to the initiation of DNA replication in Xenopus egg extracts. Genes Dev. 22 (14), 1894-1905 (2008)
ホームページへ
Hayashi, M., Katou, Y., Itoh, T., Tazumi, A., Yamada, Y., Takahashi, T., Nakagawa, T., Shirahige, K. and Masukata, H.
Genome-wide localization of pre-RC sites and identification of replication origins in fission yeast. EMBO J.26, 1327-1339 (2007); doi: 10.1038/sj.emboj.7601585
ホームページへ
Yabuuchi, H., Yamada, Y., Uchida, T., Sunathvanichkul, T., Nakagawa, T. and Masukata, H.
Ordered assembly of Sld3, GINS and Cdc45 is distinctly regulated by DDK and CDK for activation of replication origins. EMBO J. 25, 4663-4674 (2006).
ホームページへ
Nitani, N., Nakamura, KI., Nakagawa, C., Masukata, H. and Nakagawa, T.
Regulation of DNA Replication Machinery by Mrc1 in Fission Yeast. Genetics, 174, 155-165 (2006).
ホームページへ
Yamada, Y., Nakagawa, T. and Masukata, H.
A novel intermediate in initiation complex assembly for fission yeast DNA replication. Mol. Biol. Cell, 15, 3740-3750 (2004).
ホームページへ
Mazina OM, Mazin AV, Nakagawa T, Kolodner RD, Kowalczykowski SC.
Saccharomyces cerevisiae Mer3 helicase stimulates 3'-5' heteroduplex extension by Rad51; implications for crossover control in meiotic recombination. Cell 117, 47-56 (2004)
Ono, Y., Tomita, K., Matsuura, A., Nakagawa, T., Masukata, H., Uritani, M., Ushimaru, T. and Ueno, M.
A novel allele of fission yeast rad11 that causes defects in DNA repair and telomere length regulation. Nucle. Acids Res. 31, 7141-7149 (2003).
ホームページへ
Takahashi, T., Ohara, E., Nishitani, H. and Masukata, H.
Multiple ORC-binding siters are required for efficient MCM loading and origin firing in fission yeast. EMBO J. 22, 964-974 (2003).
ホームページへホームページへ
Nakajima, R. and Masukata, H.
SpSld3 is required for loading and maintenance of SpCdc45 on chromatin in DNA replication in fission yeast. Mol. Biol. Cell. 13, 1462-1472 (2002).
ホームページへ
Nakagawa, T. and Kolodner, R.D.
The MER3 DNA helicase catalyzes the unwinding of holliday junctions. J. Biol. Chem., 277, 28019-28024 (2002).
Nakagawa, T. and Kolodner, R.D.
Saccharomyces cerevisiae Mer3 is a DNA helicase involved in meiotic crossing over. Mol. Cell. Biol, 22, 3281-3291 (2002).
Takahashi, T and Masukata, H.
Interaction of fission yeast ORC with essential adenine/thymine stretches in replication origins. Genes Cells. 6, 837-849 (2001).
ホームページへ
Nakagawa, T., Flores-Rozas, H. and Kolodner, R.D.
The MER3 helicase involved in meiotic crossing over is stimulated by single-strand DNA-binding proteins and unwinds DNA in the 3' to 5' direction. J. Biol. Chem. 276, 31487- 31493 (2001).
Ogawa Y, Takahashi T, Masukata H.
Association of fission yeast Orp1 and Mcm6 proteins with chromosomal replication origins.Mol Cell Biol. 19, 7228-36 (1999).
ホームページへ
Okuno Y, Satoh H, Sekiguchi M, Masukata H.
Clustered adenine/thymine stretches are essential for function of a fission yeast replication origin.Mol Cell Biol. 19, 6699-709 (1999).
ホームページへ
Masukata H, Tomizawa J.
A mechanism of formation of a persistent hybrid between elongating RNA and template DNA.Cell. 27;62(2):331-8 (1990).
Masumoto H, Masukata H, Muro Y, Nozaki N, Okazaki T.
A human centromere antigen (CENP-B) interacts with a short specific sequence in alphoid DNA, a human centromeric satellite. J Cell Biol.109(5):1963-73 (1989).
Masukata H, Dasgupta S, Tomizawa J.
Transcriptional activation of ColE1 DNA synthesis by displacement of the nontranscribed strand.Cell. 51(6):1123-30 (1987).
Dasgupta S, Masukata H, Tomizawa J.
Multiple mechanisms for initiation of ColE1 DNA replication: DNA synthesis in the presence and absence of ribonuclease H. Cell. 51(6):1113-22 (1987).
Tomizawa J, Masukata H.
Factor-independent termination of transcription in a stretch of deoxyadenosine residues in the template DNA.Cell. 51(4):623-30 (1987).
Masukata H, Tomizawa J.
Control of primer formation for ColE1 plasmid replication: conformational change of the primer transcript. Cell. 44(1):125-36 (1986).
Masukata H, Tomizawa J.
Effects of point mutations on formation and structure of the RNA primer for ColE1 DNA replication. Cell. 36(2):513-22 (1984).
総説
升方久夫 (2009). 複製開始点活性化の時間的・空間的制御のしくみ. 蛋白質核酸酵素. 54 (4) 356-363.
升方久夫, 林真理 (2008). 染色体DNA複製開始点のゲノムワイド動態と活性化タイミング. 細胞工学. 27 (10) 967-973.
升方久夫, 林真理 (2007). 分裂酵母染色体複製開始点の網羅的解析. 実験医学. 25 (5)増刊, 596-602.
林真理, 升方久夫 (2006). 染色体維持におけるDNA複製の制御と役割:DNA複製から染色体へ. 蛋白質 核酸 酵素. 51, 2117-2122.
柳原玲子, 升方久夫 (2000). 真核細胞の複製開始点とタンパク質相互作用. 実験医学. 18, 940-948.
高橋達郎, 升方久夫(1999). DNA複製開始に機能する蛋白質複合体. 蛋白質 核酸 酵素. 44, 1804-1812.
著書
ベーシック分子生物学 (米崎哲朗・升方久夫・金澤浩著、化学同人、2014)
Fundamental Aspects of DNA Replication (open access book)
Regulation of Minichromosome Maintenance (MCM) Helicase in Response to Replication Stress.(2011) by Faria Zafar and Takuro Nakagawa
ホームページへ
分子生物学 (深見泰夫編著、化学同人、2011)
生命科学 (柳田充弘他編集、東京化学同人、2004)
The Molecular Biology of Schizosaccharomyces pombe (Richard Egel Ed. Springer, 2004)
ゲノムの複製と分配(松影昭夫、正井久雄編、III複製の開始 シュプリンガーフェアラーク東京、2002)
基礎生化学実験法 第4巻「核酸・遺伝子実験 I.基礎編」p93-117, 東京化学同人(2000)
(c)2006 Labolatory of Molecular Genetics