コンテンツ
研究紹介
生命の本質は、自らと同じ細胞を産生し、増殖することにある。太古の地球に誕生した生命は、長い変遷のうちに、遺伝情報であるDNAを正確に複製し、複製途中や外的要因によって発生するDNA障害を修復・組換えによって克服し、DNAを子孫の娘細胞に均等に継承していくシステムを獲得した。これらの反応を可能にするDNAと結合タンパク質の複合体が染色体であり、染色体機能を解明することが生命の本質の理解につながると考えている。当研究グループでは、生命の基本的しくみをより深く理解するために、分子生物学的解析に適した分裂酵母Schizosaccharomyces pombeとアフリカツメ ガエルXenopus laevis卵無細胞系を用いて、DNA複製、組換え、修復、姉妹染色体接着のしくみの解明と、セントロメアやテロメア機能の解明を目指している。
(last updated 2013.09.25)
真核生物染色体の複製開始機構
~細胞周期とクロマチン構造による複製制御~
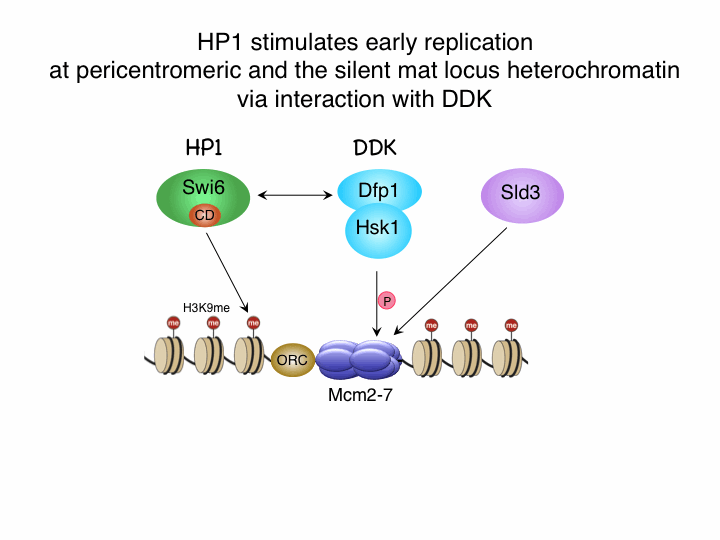
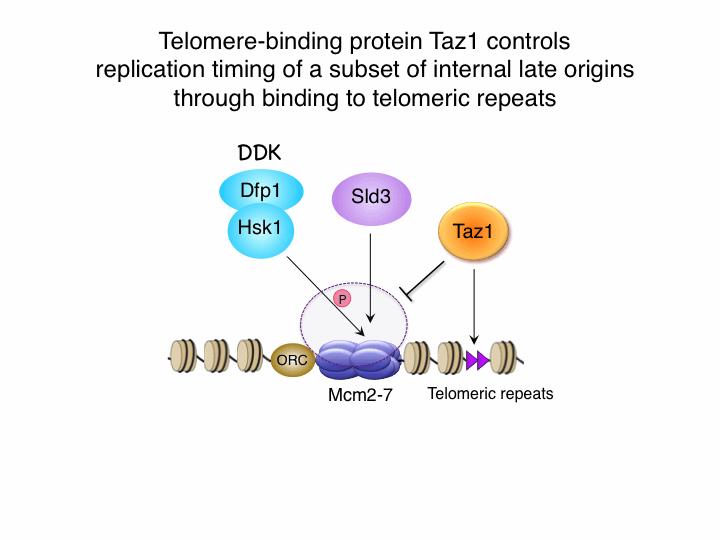
真核生物のDNA複製は染色体上の決まった場所(複製開始点 Replication originと呼ぶ)から始まる。ヒト染色体では数万個、分裂酵母では数百存在する複製開始点には、細胞周期に制御されて複製タンパク質が結合し、両方向に進行する複製フォークを形成する。染色体上では、特定の機能を担うセントロメアやテロメアをはじめ、異なる染色体構造が形成され、染色体維持や遺伝子発現調節に寄与する。限られたS期の時間内さまざまの染色体構造をもつ領域をすべてに完全に複製するために、複製開始はどのように分布し、またそれぞれの複製開始点の活性はどのように制御されているのであろうか。これらの問題に答えるために、真核生物のモデル系として優れている分裂酵母を用いて、染色体全域の複製開始点を決定し、それぞれの部位での活性制御機構を明らか にする研究を進めている。網羅的解析から、G1期にpre-replicative complex (pre-RC)を形成する部位460ヶ所を決定し、それらの約2/3はS期初期に複製が開始する初期複製開始点(下図上、赤色)であり、1/3はS期初期に複製が抑制されている後期複製開始点(下図上、青色)であることを明らかにした(Hayashi et al. 2007)。多くの生物で、ユークロマチンはS期初期に複製し、ヘテロクロマチン構造領域は遅く複製することが観察されている。しかしながらこれらのクロマチン構造が一義的に複製開始時期を決定するわけではないことが明らかとなった。分裂酵母セントロメアヘテロクロマチンと性決定領域(mat)ヘテロクロマチンでは、S期初期に活発に複製を開始する。これらの領域ではヘテロクロマチン蛋白質Swi6(ヒトHP1に相当)が、複製開始に必要なS期キナーゼであるDDKと相互作用してDDKを呼び込み、Sld3などの複製開始因子の結合を促進することを明らかにした(下図中、Hayashi et al. 2009)。いっぽう、サブテロメアヘテロクロマチン領域や腕部ユークロマチン領域の後期複製開始点では、どのようにして複製タイミングが制御されているのだろうか。一群の腕部後期複製開始点の近傍には2コピーのテロメア配列が存在し、そこにテロメア結合タンパク質Taz1が結合することがS期初期での複製開始を抑制することを発見した(下図下、Tazumi et al. 2012)。このしくみにおいてもDDKに依存するSld3の複製開始点結合が制御されることは非常に興味深い。現在は、Taz1や他のテロメア結合タンパク質がどのようにして複製タイミングを制御するかのしくみを研究している。

分裂酵母複製開始点の網羅的同定
分裂酵母第1染色体(5.5 Mb)の複製開始点を網羅的に同定し、S期初期に複製開始する初期複製開始点(赤丸)と初期に開始しない後期複製開始点(青丸)分けて表示した。
複製開始の分子機構
~複製開始の分子メカニズムの解明に向けて~
真核生物では、細胞周期のS期にゲノム全体をただ一度だけ複製するために、各複製開始点における複製開始反応は巧妙に制御されている。そのしくみを明らかにするために分裂酵母を用いて、複製に関与する因子の高温感受性変異株やオーキシン誘導的タンパク質分解(auxine-inducible-degron; AID, Kanke et al. 2011)系を用いて、解析を行ってきた。複製開始点を認識結合するORC (origin recognition complex)に依存して、サイクリン依存キナーゼCDK活性の低いG1期にのみ、Mcm2-7(minichromosome maintenance 2-7)複合体が2量体として結合する(pre-replicative complex, pre-RC)。Mcm2-7はDNA二重鎖を開裂するヘリカーゼの本体であるが、この段階では不活性である。S期移行時にMcm2-7をリン酸化するDDK (Dbf4依存キナーゼ、別名Cdc7キナーゼ)に依存してSld3がMcm2-7に結合し、さらにCDK活性の上昇に依存してSld3, Sld2がリン酸化され(Fukuura et al. 2011)、GINS (go-ichi-nii-san)複合体やCdc45が結合してヘリカーゼ活性をもつCMG複合体を形成する。CMGヘリカーゼにより複製開始点DNAがほどかれ、一本鎖DNA結合タンパク質RPAと複製DNAポリメラーゼPol alpha, Pol deltaが結合して複製を開始する。最近、我々は、複製開始点でのDNA unwindingにはにCMG複合体が形成されることに加え複製必須因子Mcm10が必須の機能をすることを明らかにした(Kanke et al. 2012)。さらにリーディング鎖を合成するDNA Pol epsilonが複製開始点でのCMG複合体形成と複製フォークでのCMGヘリカーゼ進行促進に必須機能を持つことを明らかにした(Handa et al. 2012)。
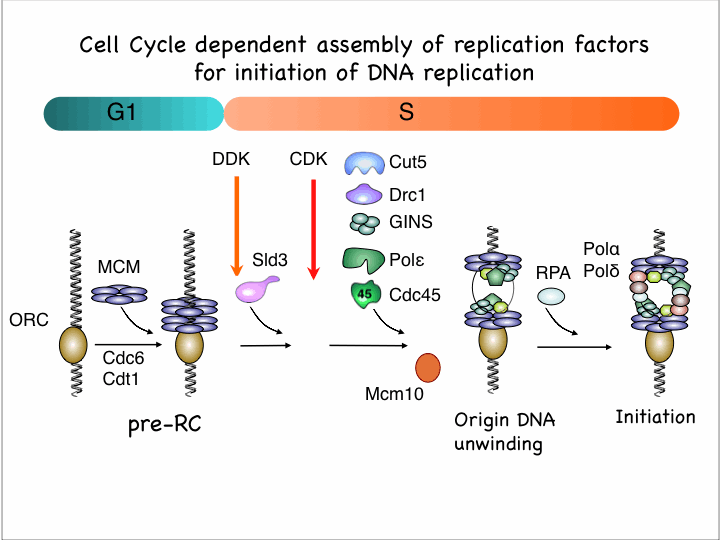
複製開始因子の集合過程
真核生物染色体の複製開始機構
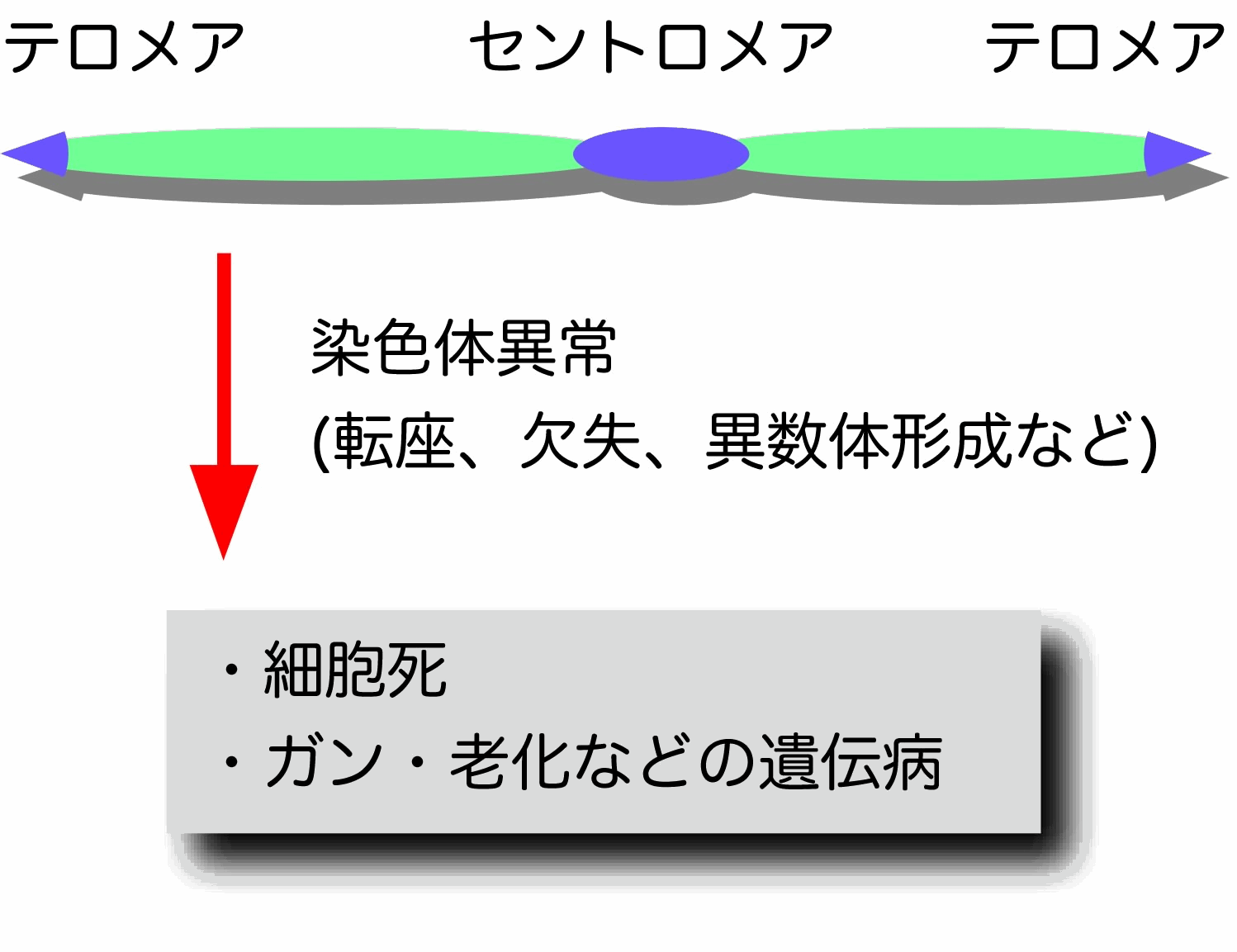
ヒトを含む真核生物のゲノムには多くのリピート配列が存在する。それら相同配列の間で染色体再編が起こると転座や同腕染色体などの異常染色体が生じる。染色体異常は細胞死やガン・老化などの遺伝病を引き起こすことから、このような組換え反応は厳密に制御されなければならない。我々は、染色体改変が比較的容易な分裂酵母を用いて、染色体維持やゲノム進化に於いて極めて重要なセントロメア領域で起こるDNA相同組換えの分子メカニズムとその制御機構の解明を目指している。
真核生物染色体の複製開始機構
~染色体の正確な分配を保証するメカニズム~
染色体継承の仕組みは、DNAを正確に複製する機構と、染色体を正確に分配する機構により支えられている。我々は、これらの機構のうち、DNA塩基情報の合成エラーを修復するDNAミスマッチ修復機構と、染色体分配やDNA二重鎖切断修復を支える染色体接着機構に注目し、その動作機構の解明を目指している。現在、ツメガエル卵抽出液を用いた生化学的解析により、これら二つの反応がDNA複製機構と協調して機能するメカニズムを明らかにしつつある。
(c)2009 Labolatory of Molecular Genetics